Nóng: Bộ Y tế thông tin về việc lưu hành, sử dụng thuốc Evusheld tại Việt Nam
Hội đồng tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc của Bộ Y tế đã tổ chức họp khẩn cấp vào ngày 31/01/2023 để xem xét về việc lưu hành, sử dụng thuốc Evusheld tại Việt Nam.
Chiều ngày 3/2, Cục Quản lý Dược - Bộ Y tế đã có thông tin về sinh phẩm Evusheld.
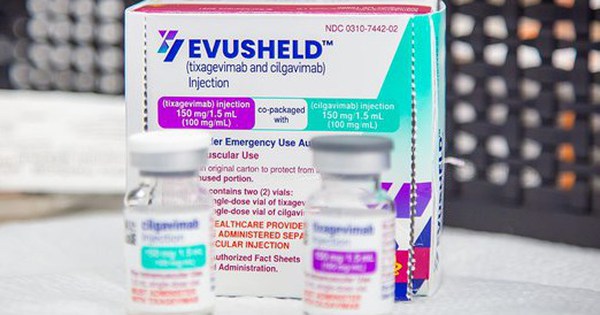
Theo Cục Quản lý Dược, Evusheld là sinh phẩm kết hợp bộ đôi kháng thể đơn dòng (tixagevimab 150mg/1,5ml và cilgavimab 150mg/1,5ml) được AstraZeneca phát triển với chỉ định dự phòng trước phơi nhiễm COVID-19 ở người lớn và thanh thiếu niên từ 12 tuổi trở lên có trọng lượng ít nhất 40kg.
Evusheld đã được cấp phép lưu hành bởi nhiều cơ quan quản lý, bao gồm các hình thức cấp phép lưu hành có điều kiện, cấp phép sử dụng khẩn cấp và các hình thức khác nhằm hỗ trợ tiếp cận sớm với thuốc (Early access) và hiện Evusheld đã được sử dụng tại gần 40 quốc gia trên thế giới với chỉ định điều trị và/hoặc dự phòng phơi nhiễm COVID-19.
Tại Việt Nam, Cục Quản lý Dược cho biết thuốc Evusheld đã được cấp giấy đăng ký lưu hành ngày 25/10/2022.
Bộ Y tế đã tổ chức họp khẩn cấp để xem xét về việc lưu hành, sử dụng thuốc Evusheld tại Việt Nam.
Ngày 26/01/2023, Cơ quan quản lý thực phẩm và dược phẩm Hoa Kỳ (USFDA) có thông báo tạm dừng cấp phép sử dụng trong trường hợp khẩn cấp thuốc Evusheld cho tới khi có thông báo cập nhật của USFDA với lý do Evusheld không có tác dụng bảo vệ đối với một số biến chủng mới của SARS-CoV-2 hiện đang chiếm ưu thế tại Hoa Kỳ, như biến chủng phụ XBB.1.5 của Omicron (hiện có hơn 90% ca nhiễm do biến chủng này tại Hoa Kỳ).
Theo USFDA, việc sử dụng Evusheld sẽ bị giới hạn cho đến khi tỷ lệ biến chủng SARS-CoV-2 không nhạy cảm với Evusheld ở Hoa Kỳ giảm xuống dưới 90%.
Ngoài ra, USFDA khuyến cáo các cơ sở y tế và nhà cung cấp Evusheld vẫn nên giữ lại các chế phẩm hiện có để bảo quản theo quy định và sử dụng trong trường hợp các biến chủng của SARS-CoV-2 mà Evusheld chống lại được trở nên phổ biến hơn ở Hoa Kỳ.
Cho đến thời điểm ngày 30/01/2023, Evusheld vẫn được cho phép lưu hành, sử dụng bởi các Cơ quan quản lý dược chặt chẽ (SRA) như EMA, Nhật Bản, Anh, Úc, Canada, Thuỵ Sĩ… và tại các nước khu vực châu Á như: Nhật Bản, Hồng Kông, Maylasia, Thái Lan, Singapore, Đài Loan.
Cục Quản lý Dược cho biết, ngay sau khi nhận được thông tin nêu trên từ USFDA, Hội đồng tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc của Bộ Y tế đã tổ chức họp khẩn cấp vào ngày 31/01/2023 để xem xét về việc lưu hành, sử dụng thuốc Evusheld tại Việt Nam.
Trên cơ sở báo cáo, thông tin về các biến chủng của virus SARS-COV-2 đang lưu hành tại Việt Nam, tình hình cấp phép, sử dụng Evusheld trên thế giới, cảnh báo của Tổ chức Y tế Thế giới (WHO) về đại dịch COVID-19 hiện vẫn là tình trạng khẩn cấp toàn cầu đối với sức khỏe cộng đồng,
Hội đồng đã kết luận:
- Thông tin báo cáo cập nhật đến ngày 19/01/2023 cho thấy xu hướng thay đổi về biến chủng XBB của Omicron tại châu Á hiện nay chỉ chiếm tỉ lệ khoảng 2-5% các trường hợp nhiễm SARS-COV-2 và tỉ lệ này hiện nay của Việt Nam khoảng 3%.
- Thuốc Evusheld hiện vẫn có tác dụng đối với các biến chủng của virus SARS-COV-2 đang lưu hành phổ biến tại Việt Nam (tại miền Bắc thông tin về tình hình giải trình tự gen các ca bệnh COVID-19 trên 541 mẫu thực hiện tại Viện Vệ sinh dịch tễ Trung ương, từ tháng 6- 11, biến thể BA5 chiếm ưu thế, bên cạnh đó ghi nhận một số biến thể phụ khác như BA.2.74, BE.1.1; Tháng 12, biến thể phụ BN.1.3 chiếm ưu thế; tiếp đó là các biến thể phụ BA.5.2, BA.2.75.6…).
- Ngoại trừ USFDA dừng cấp phép sử dụng do tình hình thực tiễn của các biến chủng SARS-COV-2 lưu hành tại Hoa Kỳ, Evusheld hiện vẫn đang được cho phép lưu hành, sử dụng bởi các Cơ quan quản lý dược chặt chẽ (SRA) như EMA, Nhật Bản, Anh, Úc, Canada, Thuỵ Sĩ… và nhiều cơ quan quản lý dược trên thế giới.
Vì vậy, trên cơ sở phân tích tác dụng của thuốc với các biến chủng lưu hành tại Việt Nam và việc lưu hành, sử dụng thuốc tại các nước trên thế giới, Hội đồng thống nhất đề xuất tiếp tục cho phép lưu hành, sử dụng thuốc Evusheld tại Việt Nam đồng thời tiếp tục theo dõi, giám sát chặt chẽ và cập nhật thông tin về tính an toàn, hiệu quả của thuốc đối với các biến chủng của virus SARS-COV-2 tại các nước trên thế giới và Việt Nam.
Mệt mỏi, sụt cân sau thời gian dài táo bón, người phụ nữ 48 tuổi nhận kết quả không ngờ
Y tế - 5 ngày trướcGĐXH – Bản thân bệnh nhân nghĩ rằng do táo bón kéo dài dẫn đến chảy máu. Tuy nhiên, khi đi khám, kết quả nội soi đã khiến chị bất ngờ.
Người phụ nữ 67 tuổi ở Hà Nội mang khối u gan phình gấp 10 lần chỉ sau vài tháng dùng thuốc nam truyền miệng
Y tế - 1 tuần trướcGĐXH - Từ một khối u nhỏ chỉ 2 cm, người bệnh cho rằng chưa nguy hiểm nên đã quyết định tự điều trị tại nhà bằng thuốc nam không rõ nguồn gốc. Sau vài tháng, khối u tăng lên 20cm, hoại tử, buộc phải cắt gần một nửa lá gan.
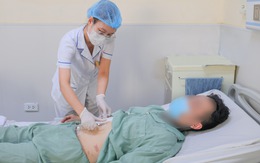
Quả thận 'dập nát' của nam bệnh nhân 31 tuổi được bác sĩ đưa ra ngoài cơ thể rồi ghép lại thành công
Y tế - 1 tuần trướcGĐXH - Sau tai nạn giao thông nghiêm trọng, nam bệnh nhân 31 tuổi đứng trước nguy cơ mất quả thận phải suốt đời. Tuy nhiên, bằng kỹ thuật ghép thận tự thân đầu tiên, các bác sĩ đã “hồi sinh” thành công quả thận từng bị đứt rời và dập nát nặng.
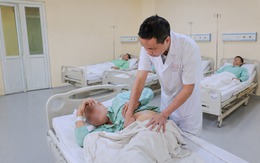
Ca can thiệp tán sỏi hiếm gặp: Thận 'chui lên ngực', cột sống gập cứng khiến đường vào gần như bị khóa kín
Y tế - 1 tuần trướcGĐXH - Một ca tán sỏi qua da đặc biệt vừa được các bác sĩ khoa Phẫu thuật Tiết niệu và Nam học, Bệnh viện E thực hiện thành công cho người bệnh nam 65 tuổi có biến dạng cột sống nghiêm trọng suốt gần 20 năm.
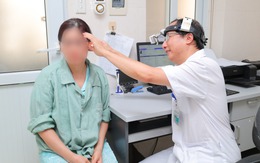
Người phụ nữ nghe kém suốt 2 năm, bác sĩ phát hiện xương nhỏ nhất cơ thể bị 'đóng cứng'
Y tế - 2 tuần trướcGĐXH - Sau nhiều năm sống trong tình trạng nghe kém kéo dài, một phụ nữ 46 tuổi đã dần phục hồi sức nghe sau ca phẫu thuật nội soi thay thế xương bàn đạp bằng trụ gốm sinh học tại Bệnh viện E.
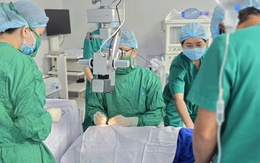
Bé trai 10 tuổi gần như chỉ thấy sáng tối, cải thiện thị lực sau phẫu thuật đục thủy tinh thể
Y tế - 2 tuần trướcGĐXH - Một bệnh nhi 10 tuổi mắc đục thủy tinh thể bẩm sinh kèm bệnh lý võng mạc trẻ sinh non vừa được phẫu thuật thành công, cải thiện đáng kể thị lực sau nhiều năm nhìn mọi thứ trong tình trạng mờ nhòe.
Ngày Dinh dưỡng cộng đồng Việt Nam lần thứ 6: Đưa lối sống lành mạnh đến gần hơn với người dân
Y tế - 2 tuần trướcNgày Dinh dưỡng cộng đồng Việt Nam lần thứ 6 khai mạc trong không khí sôi động, rực rỡ sắc màu. Hàng nghìn người dân cùng 20 đội chơi tham gia các hoạt động vận động, khám tư vấn sức khỏe và trình diễn tập thể, lan tỏa tinh thần sống khỏe, năng động và gắn kết cộng đồng.
Người dân hào hứng khám sức khỏe miễn phí tại Ngày Dinh dưỡng cộng đồng Việt Nam lần 6
Y tế - 2 tuần trướcSKĐS - Hàng nghìn người dân TPHCM đã tham gia thăm khám, kiểm tra thể trạng và nhận tư vấn dinh dưỡng miễn phí từ các chuyên gia, bác sĩ tại Ngày Dinh dưỡng cộng đồng Việt Nam lần thứ 6 tại Dinh Thống Nhất.

Loại quả nhiều người chê 'nhạt nhẽo' lại là kho dưỡng chất 'vàng' cho tim mạch và đôi mắt
Bệnh thường gặp - 2 tuần trướcGĐXH - Theo ThS.BS Nguyễn Vũ Bình, bí ngòi không chỉ là thực phẩm dễ chế biến mà còn chứa nhiều dưỡng chất có lợi cho cơ thể. Từ hỗ trợ thị lực, tăng cường sức khỏe tim mạch đến cải thiện tiêu hóa và bổ sung chất chống oxy hóa, bí ngòi được xem là lựa chọn tốt cho chế độ ăn uống lành mạnh hằng ngày.
Chính thức: Hỗ trợ tối thiểu 2 triệu đồng cho phụ nữ sinh đủ 2 con trước 35 tuổi
Dân số và phát triển - 3 tuần trướcChính phủ ban hành Nghị định số 168/2026/NĐ-CP quy định chi tiết một số điều và biện pháp tổ chức, hướng dẫn thi hành Luật Dân số. Một trong những nội dung đáng chú ý của nghị định là phụ nữ sinh đủ 2 con trước 35 tuổi được hỗ trợ tối thiểu 2 triệu đồng từ năm 2027.

Loại quả nhiều người chê 'nhạt nhẽo' lại là kho dưỡng chất 'vàng' cho tim mạch và đôi mắt
Bệnh thường gặpGĐXH - Theo ThS.BS Nguyễn Vũ Bình, bí ngòi không chỉ là thực phẩm dễ chế biến mà còn chứa nhiều dưỡng chất có lợi cho cơ thể. Từ hỗ trợ thị lực, tăng cường sức khỏe tim mạch đến cải thiện tiêu hóa và bổ sung chất chống oxy hóa, bí ngòi được xem là lựa chọn tốt cho chế độ ăn uống lành mạnh hằng ngày.